2eme partie: ORGANISATION ET TRANSFORMATION DE LA MATIERE
CHAP I :
CONSTITUTION DE LA MATIERE
1) La masse volumique et la solubilité :
La masse volumique r d’un corps est le quotient
de la masse m du corps par son volume V. Elle se note r. La relation s’écrit :
r = m/V
(r en
kg/L, m en kg et V en L) ou m=rxV ou V=m/r
activité expérimentale :
mesure de la masse volumique d'un corps
La solubilité s d’un
corps est le quotient de la masse maximale mmax
de soluté que l’on peut dissoudre par le volume V de mélange obtenu :
s = mmax/V (s en g/L, mmax
en g et V en L) ou mmax=sxV
ou V=mmax/s
activité expérimentale :
mesure de la solubilité d'un soluté
2) Des atomes et des ions :
Un atome est constitué d’un noyau et d’électrons en mouvement autour du
noyau.
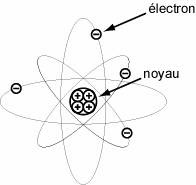
Le diamètre du noyau est environ 100000 fois plus petit que le diamètre de l’atome (de taille moyenne 1/10 nm) : la matière est donc constituée essentiellement de vide.
La charge négative des électrons compense la charge positive du
noyau : l’atome est donc électriquement neutre.
Un ion est un atome ou un groupe d’atomes qui a
perdu ou gagné des électrons.
Lorsque l’atome, qui est électriquement neutre, perd 1, 2
ou 3 électrons dont la charge est négative, on obtient alors un ion positif
Exemple : ion
aluminium Al3+
Lorsque l’atome, qui est électriquement neutre, gagne 1,
2 ou 3 électrons dont la charge est négative, on obtient alors un ion négatif
Exemple : ion chlorure Cl- ou l’ion sulfate
SO42-
Ions polyatomiques:
Certains ions peuvent être constitués d'un groupement d'atomes. Se sont des ions polyatomiques. Exemple : ion sulfate
SO42-
Identification des ions:
On peut identifier certains ions présents en
solution aqueuse à l’aide de réactifs. C’est le cas des ions chlorure Cl- qui
réagissent avec le nitrate d'argent et des ions métalliques (ions fer II Fe2+, ions fer III Fe3+, ions cuivre Cu2+) qui réagissent avec
de l’hydroxyde de sodium (soude). Dans ce cas, il se forme un précipité de couleur caractéristique de l’ion testé
Activité
expérimentale :
tests de reconnaissance des ions